
|
|
|
テーマ:暮らしを楽しむ(384408)
カテゴリ:薬の話
承認年
1971年 開発の経緯 キロサイド注はシタラビン(Ara-C)を成分とする代謝拮抗剤であり、DNA合成阻害に基づく抗腫瘍作用を有する。 シタラビンは1959年にアメリカで、Walwickらによって最初に合成され、1961年Evansらが動物腫瘍に対する抑制作用を認めて以来、抗腫瘍剤として注目されるようになった。1962年にTalleyらはシタラビンを初めて人体に投与して癌における有効性を明らかにし、1965年にはCareyらが急性白血病に応用し、著明な抗白血病作用を有することが明らかになった。 我が国においては、キロサイド注が白血病治療剤として1971年に販売を開始し、1973年に他の抗腫瘍剤との併用により固形癌(消化器癌、肺癌、乳癌、女性性器癌等)に対する適応が、1984年に膀胱内への注入療法による膀胱腫瘍に対する適応がそれぞれ追加された。1991年12月12日には薬事法第14条第2項各号(承認拒否事由)のいずれにも該当しないとの再審査結果を得た。2006年2月には医療事故防止対策のため販売名を変更し、新たな製造販売承認を得た。2014年4月には薬事法第14条第2項各号(承認拒否事由)のいずれにも該当しないとの再評価結果を得た。 2014年12月18日に髄腔内化学療法に対する用法・用量の変更に係る一部変更承認、2020年8月21日に、公知申請によりシタラビン少量療法の用法用量に係る一部変更承認を得た。
製品の治療学的特性 ① 急性白血病に寛解導入・維持療法及び髄腔内化学療法で効果を示す。 ② 固形癌に多剤併用療法で効果を示す。 ③ 膀胱腫瘍に膀胱内注入療法で効果を示す。 ④ 副作用 重大な副作用は、骨髄機能抑制に伴う血液障害、ショック、消化管障害、急性呼吸促迫症候群、間質性肺炎、急性心膜炎、心のう液貯留、中枢神経系障害が報告されている。(「Ⅷ. 安全性(使用上の注意等)に関する項目 8.副作用」の項参照) 販売名 和名 キロサイド注20mg、キロサイド注40mg、キロサイド注60mg、キロサイド注100mg、キロサイド注200mg 洋名 Cylocide Injection 20mg、Cylocide Injection 40mg、Cylocide Injection 60mg、Cylocide Injection 100mg、Cylocide Injection 200mg 名称の由来 Cytosine arabinosideより命名 一般名 和名(命名法) シタラビン(JAN) 洋名(命名法) Cytarabine(JAN) ステム -(ar)abine:アラビノフラノシル誘導体 引用:キロサイド・インタビューフォーム 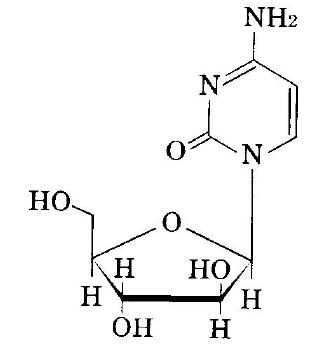  【送料無料】 ホップ・ステップ・ジャンプで進めるがん治療の薬薬連携(Cd-rom付き): 保険薬剤師・病院薬剤師のための外来抗がん薬の業務ガイダンス / 日本臨床腫瘍薬学会 【本】 お気に入りの記事を「いいね!」で応援しよう
Last updated
2021.10.23 07:23:26
コメント(0) | コメントを書く
[薬の話] カテゴリの最新記事
|