
|
|
|
カテゴリ:虫歯の電気化学説
 虫歯ができるどころか、溶解さえしないという実験結果を得たので、 虫歯は単なる酸蝕症ではなく、別のメカニズムがあると考えた。 そうでないと、虫歯については理解できないことが多すぎるからだ。 そこで、虫歯は金属腐食と同じ電気化学的腐食ではないかと考え、 その前提として歯牙に電極を取り付け電流が流れるか調べてみた。 pH3の塩酸中に歯牙を浸漬し、 12.7Vの印加電圧で100μAの電流が流れた。 この実験では、歯牙の電気的抵抗は127kΩとなり、 充分な電導性がある、 つまり歯牙は金属として取り扱うことができるという結論を得た。 また歯牙はリン酸とCa(カルシウム:アルカリ金属)から構成されているので、 電導性があることは充分考えられる。 金属腐食の分野では金属腐食の原因、その対処法に関する研究は進んでいる。 なぜなら、金属の腐食による経済的損失はGDPの5%にも達すると言われていて、危急の問題だからだ。 金属腐食の分野ではすでにバイオフィルが関係する金属腐食の研究も進んでいて、「微生物腐食」という名称が確立している。 詳しくは、当サイトの「虫歯予防一口メモ」の過去ログを参照していただくとして、 今日は、金属腐食の電気化学式による解説を試みたい。 表題の図での解説に入る前にいわゆる酸蝕の電気化学式を 書いておく、 酸蝕には電極は存在しない、 金属Mから電子e-が奪われ、水素イオンH+と結びつき水素ガスH2↑となる、一方電子e-を奪われた金属MはM+(金属イオン)となって溶出する。 M→M++e-、2H++2e-→H2↑ 表題図では2つの金属電極が存在し、その電極同士は電気的に接続されている。 電子e-を奪われた側の電極が溶出するが、 2種の金属を比べた場合、 相対的にイオン化傾向の高い方が低いほうに電子e-を奪われ溶出する。 これが左図だ。 歯牙の場合は陽極がエナメル質、陰極が象牙質となり 象牙質だけが溶出する。 これは蓄電池の構造そのものであり、 電気的に接続している2種の金属電極の途中に電球をつなげば光る。 これら電気化学的腐食(腐食電池)が単なる酸蝕と決定的に異なる点は、 持続的に電子e-の供給が起こり、 その腐食効率は単なる酸蝕に比べて非常に高いということである。 特に問題が大きいのは右図の「酸素消費型の腐食」だ、 2種の金属電極のイオン化傾向の違いだけではなく、 酸素濃度勾配によりこの腐食メカニズムが促進されることが示されている。 隙間の外の陰極となる金属表面では、 酸素濃度が高いため、 O2+4H++4e-→2H2O ~1式 O2+2H2O+4e-→4OH- ~2式 という反応が持続的に起こり、 電子e-を奪われた陽極は溶出(腐食)する。 一般に酸素濃度はすき間の奥ほど低い傾向があり、 また微生物はすき間の奥に生息している、 また微生物は我々人間と同じ酸素呼吸をしているので その活動を支えるため酸素を消費する。 したがって、すき間の奥は酸素濃度が低く、 一方外は相対的に酸素濃度は高いので 奥外に大きな酸素濃度勾配を形成する。 酸素濃度が高い方が陰極となり電子e-を奪い、 酸素濃度が低い方が陽極となり電子e-を奪われ溶出(腐食)する。 これは「濃淡電池」と呼ばれ古くから知られており、 同じ現象を腐食の観点から見れば「通気差腐食」となる。 具体的には、すき間の奥の方が電子e-を奪われ腐食する。 これがいわゆる「咬合面の小窩裂溝ウ蝕」だ。 「咬合面の小窩裂溝ウ蝕」とは穴の内外に「濃淡電池」という局部電池を形成しているので、 持続的に電子e-が穴の奥から奪われ腐食することにより、 その穴は次第に深くなる。 また微生物は糖質を供給されると解糖酵素により 酸素を消費しつつATPと乳酸等の有機酸(H+)を生成する。 1式を見ていただくと分かるが、 H+(水素イオン:酸)があると1式の反応は進む、 つまり酸性環境下で腐食反応は進む。 腐食の原因は酸素濃度勾配と前出のイオン化傾向の違いだけではないのだ。 虫歯とは単なる酸蝕症ではなく、 金属腐食(電気化学的腐食)だということがお解かりいただけたと思う。 2式での生成物はOH-(水酸イオン:アルカリ)なので、 H+と拮抗している。 つまりH++OH-→H2Oとなって、 この中和反応の終了と共に、この一連の反応は拮抗し停止する。 ここに虫歯抑制のヒントがある。 OH-を外部から供給するか、 またはH+を除去することにより、 1式も2式も止まる、酸アルカリの中和反応だ。 止まるだけではない、逆反応も起りうる。 つまり、虫歯が抑制されるだけではなく、 虫歯が治るかもしれないのだ。 また、虫歯菌の解糖酵素の至適pHは低いので、 アルカリ性環境下ではその酵素活性は低下する。 つまり酸素も消費しないし、酸も産生されない。 これは「微生物腐食」は抑制されるということだ。 しかも、再石灰化という歯牙の再結晶化はpH依存性が有り、 pHが低い(酸性)よりpHが高い(アルカリ性)方が起こりやすい。 歯牙の自己修復機能もアルカリ性環境下の方が亢進される。 ではOH-を外部から供給する、H+を除去するとは 具体的にはどういうことをすればよいのか? それは、飲食後速やかに「重曹うがい」をすることだ、 重曹はH+を消費する、水に溶かすとアルカリ性だ。 NaHCO3→Na++HCO3-、 H++HCO3-→H2O+CO2↑ いずれの電気化学的腐食のタイプにおいても、 1、電子e-を奪われない 2、水素イオンH+がない(アルカリ性)環境では腐食は起こらない。 実際Feの例だが、 不感域(腐食しない領域)は、 1、対電極に対して電位が低い(電子e-を奪われない) 2、アルカリ性領域にある場合だ。 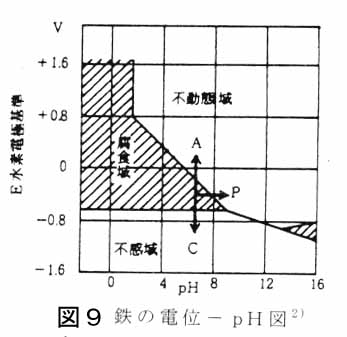 #リンク先の皆様、多謝! 参考文献:1、金属の腐食と摩擦磨耗 2、丹治研究室 Tanji Laboratory ホームページ 東京工業大学 大学院生命理工学研究科 生物プロセス専攻 生物機能工学講座 生物化学工学分野 お気に入りの記事を「いいね!」で応援しよう
Last updated
2009/11/03 05:03:17 PM
コメント(0) | コメントを書く
[虫歯の電気化学説] カテゴリの最新記事
|
|